| |
Podemos calcular a variaçăo de entalpia (DH) de uma reaçăo conhecendo os valores de energia das ligaçőes existentes entre os átomos das substâncias envolvidas na reaçăo.
Considere o exemplo: N2 (g) + 3 H2 (g)  2 NH3 (g) 2 NH3 (g)
Para formar 2 moléculas de amônia a partir de uma molécula de nitrogęnio e tręs moléculas de hidrogęnio, devemos primeiro quebrar as ligaçőes presentes nas moléculas dos reagentes em átomos livres e entăo formar novas ligaçőes a partir destes átomos:
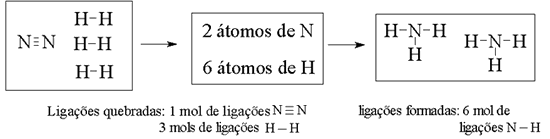
Dispondo de valores para as energias de ligaçăo, podemos calcular o DH para a reaçăo utilizando a expressăo:
A variaçăo de entalpia é obtida através do somatório das ligaçőes rompidas menos o somatório das ligaçőes formadas.
Dadas as energias de ligaçăo:
DH (N-N) = 941 kJ/mol
DH (H-H) = 436 kJ/mol
DH (N-H) = 389 kJ/mol
DH= 941 + 3.(436) - 6.(389)
DH = - 85 kJ
|
|
|